Страница 48
Белки различаются между собой по молекулярной массе, которая для большинства из них лежит в пределах 6000-1 000 000.
Белки различаются по составу на простые и сложные. Простые белки состоят только из аминокислот, содержа 50% углерода, 7% водорода, 23% кислорода, 16% азота. В состав некоторых простых белков может входить сера в небольшом количестве.
Сложные белки помимо аминокислот содержат в своем составе другие соединения как органические, так и неорганические. Эту небелковую часть молекулы сложного белка называют простетической группой. Сложными белками являются нуклеопротеиды, липопротеиды, фосфопротеиды, металлопротеиды и гликопротеиды (табл. 5).
Таблица 5
Перечень некоторых сложных белков
Вид сложного белка
Простатическая группа
Нуклеопротеиды:
Рибосомы
РНК
РНК-содержащие вирусы
Гликопротеиды:
g-глобулин
Гексозамин, галактоза, сиаловая кислота
Липопротеиды:
Липопротеиды плазмы
Фосфолипиды, холестерин, нейтральные липиды
Фосфопротеиды:
Казеин
Фосфатная группа + остаток серина
Гемопротеиды:
Гемоглобин
Железопротопорфирин
Цитохром
Железопротопорфирин
Флавопротеиды:
Сукцинатдегидрогеназа
Флавиннуклеотид
Оксидаза D-аминокислот
Флавиннуклеотид
Металлопротеиды:
Ферритин
Тирозиноксидаза
Алкогольдегидрогеназа
Белки различаются также по структуре, которая зависит от количества входящих в их состав аминокислот (аминокислотных остатков) и последовательности (чередования) аминокислот в поли-пептиде. Одни белки построены из одной (рибонуклеаза, лизоцим), двух (бычий инсулин), трех (хемотрипсин), четырех (гемоглобин человека) и более полипептидных цепей.
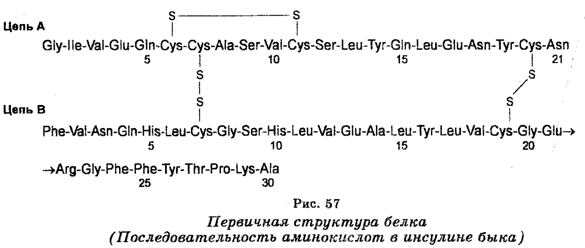
Различают первичную, вторичную, третичную и четвертичную структуру белков. Первичная структура определяется отношением одного аминокислотного остатка к другому в полипептиде, т. е. последовательностью аминокислотных остатков в полипептиде (рис. 57). Вторичная структура определяется скрученностью полипептидных цепей в виде спиралей. Третичная структура характерна для полипептидных спиральных структур, образующих клубки (фибриллы). Что касается четвертичной структуры, то она возникает, когда происходит соединение между собой нескольких молекул.
В зависимости от конформации (пространственной структуры), различают глобулярные (полипептидные цепи образуют клубки) и фибриллярные белки (полипептидные цепи формируют фибриллы). Глобулярными белками являются почти все ферменты, антитела, гормоны, гемоглобин, сывороточный альбумин, тогда как фибрил-лярными являются коллаген сухожилий и костей, кератинин волос и другие.
На долю белков в цитоплазме приходится 50-70% от общего количества органических соединений. Что же касается функций белков, то они исключительно разнообразны (табл. 6).
Белки являются, прежде всего, строительным материалом, т. к. входят в состав практически всех клеточных структур. Кроме того, обладая способностью образовывать волокна, многие белки выполняют опорную функцию. Например, основу кожи, хрящей и сухожилий у млекопитающих составляет фибриллярный белок коллаген, который при кипячении в воде превращается в желатин, а связок — эластин. Химический состав волос, ногтей (когтей) и перьев определяется в основном кератином. Шелковые нити и паутина построены из белка фибреина.
Таблица 6
Обсуждение Биология с основами Экологии
Комментарии, рецензии и отзывы
